Page 5 - Kimya 12 | Çalışma Defteri-4
P. 5
Hatırlıyor muyum?
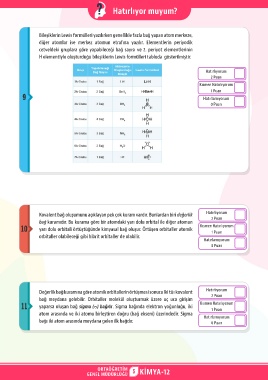
Bileşiklerin Lewis formülleri yazılırken genellikle fazla bağ yapan atom merkeze,
diğer atomlar ise merkez atomun etrafına yazılır. Elementlerin periyodik
cetveldeki gruplara göre yapabileceği bağ sayısı ve 2. periyot elementlerinin
H elementiyle oluşturduğu bileşiklerin Lewis formülleri tabloda gösterilmiştir.
Hatırlıyorum
2 Puan
Kısmen Hatırlıyorum
1 Puan
9 Hatırlamıyorum
0 Puan
Kovalent bağ oluşumunu açıklayan pek çok kuram vardır. Bunlardan biri değerlik Hatırlıyorum
2 Puan
bağ kuramıdır. Bu kurama göre bir atomdaki yarı dolu orbital ile diğer atomun
10 yarı dolu orbitali örtüştüğünde kimyasal bağ oluşur. Örtüşen orbitaller atomik Kısmen Hatırlıyorum
1 Puan
orbitaller olabileceği gibi hibrit orbitaller de olabilir.
Hatırlamıyorum
0 Puan
Değerlik bağ kuramına göre atomik orbitallerin örtüşmesi sonucu iki tür kovalent Hatırlıyorum
2 Puan
bağ meydana gelebilir. Orbitaller molekül oluşturmak üzere uç uca girişim
11 yaparsa oluşan bağ sigma (σ) bağıdır. Sigma bağında elektron yoğunluğu, iki Kısmen Hatırlıyorum
1 Puan
atom arasında ve iki atomu birleştiren doğru (bağ ekseni) üzerindedir. Sigma Hatırlamıyorum
bağı iki atom arasında meydana gelen ilk bağdır. 0 Puan
MATEMATİK-11
ORTAÖĞRETİM 5 KİMYA-12
GENEL MÜDÜRLÜĞÜ