Page 16 - Kimya 11 | Çalışma Defteri -7
P. 16
Çoktan Seçmeli
12. NO₂(g) + CO(g) → NO(g) + CO₂(g) 14. Fe(k) + 2HCl(suda) → FeCl₂(g) + H₂(g)
Tepkimesi için sabit sıcaklıkta yapılan deney sonuçları Tepkimesinde aynı miktar farklı boyutlarda demir
aşağıda verilmiştir. metali, eşit derişimli ve eşit hacimli HCl ile ayrı
ayrı tepkimeye sokuluyor. Aynı şartlarda demir
Başlangıç Tepkimenin metalinden farklı büyüklükler kullanılarak
Deneyler Derişimleri (M) Başlangıç Hızı gerçekleşen tepkimede zamanla açığa çıkan hidrojen
[NO₂] [CO] (M/s)
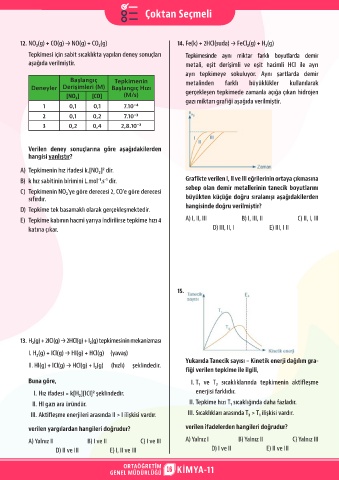
gazı miktarı grafiği aşağıda verilmiştir.
1 0,1 0,1 7.10-⁴
2 0,1 0,2 7.10-³
3 0,2 0,4 2,8.10-³
Verilen deney sonuçlarına göre aşağıdakilerden
hangisi yanlıştır?
A) Tepkimenin hız ifadesi k.[NO₂]² dir.
B) k hız sabitinin birimini L.mol-¹.s-¹ dir. Grafikte verilen I, II ve III eğrilerinin ortaya çıkmasına
sebep olan demir metallerinin tanecik boyutlarını
C) Tepkimenin NO₂’ye göre derecesi 2, CO’e göre derecesi
sıfırdır. büyükten küçüğe doğru sıralanışı aşağıdakilerden
hangisinde doğru verilmiştir?
D) Tepkime tek basamaklı olarak gerçekleşmektedir.
E) Tepkime kabının hacmi yarıya indirilirse tepkime hızı 4 A) I, II, III B) I, III, II C) II, I, III
katına çıkar. D) III, II, I E) III, I II
15.
13. H₂(g) + 2ICl(g) → 2HCl(g) + I₂(g) tepkimesinin mekanizması
I. H₂(g) + ICl(g) → HI(g) + HCl(g) (yavaş)
Yukarıda Tanecik sayısı – Kinetik enerji dağılım gra-
II. HI(g) + ICl(g) → HCl(g) + I₂(g) (hızlı) şeklindedir.
fiği verilen tepkime ile ilgili,
Buna göre, I. T₁ ve T₂ sıcaklıklarında tepkimenin aktifleşme
I. Hız ifadesi = k[H₂][ICl]² şeklindedir. enerjisi farklıdır.
II. HI gazı ara üründür. II. Tepkime hızı T₁ sıcaklığında daha fazladır.
III. Aktifleşme enerjileri arasında II > I ilişkisi vardır. III. Sıcaklıkları arasında T₂ > T₁ ilişkisi vardır.
verilen yargılardan hangileri doğrudur? verilen ifadelerden hangileri doğrudur?
A) Yalnız II B) I ve II C) I ve III A) Yalnız I B) Yalnız II C) Yalnız III
D) II ve III E) I, II ve III D) I ve II E) II ve III
ORTAÖĞRETİM 16 KİMYA-11
GENEL MÜDÜRLÜĞÜ