Page 34 - Kimya 11 | Çalışma Defteri -7
P. 34
CEVAP ANAHTARI
BECERİ TEMELLİ
1.
Yönerge:
A) N₂ ve H₂ moleküllerinden NH₃ molekülünün oluşabilmesi için etkin çarpışma yapmaları gerekir. Etkin çarpışma için uygun
geometrik biçimde ve aynı düzlemde çarpışmaları, yeterli kinetik enerjiye sahip olmaları, aktifleşmiş kompleks ürün
oluşturmaları gerekir.
B) Bir tepkimenin gerçekleşebilmesi için çarpışan taneciklerin sahip olmaları gereken minimum toplam kinetik enerjiye
aktivasyon enerjisi denir. Her kimyasal tepkimenin farklı bir aktivasyon enerjisi vardır. Bütün kimyasal tepkimeler için
aktivasyon enerjisine ihtiyaç vardır.
C)
a) H₂O oluşuyorsa; uygun geometrik biçimde ve yeterli kinetik enerjiye sahip etkin çarpışma gerçekleşmiştir.
b) H₂O oluşmuyorsa; etkin olmayan çarpışma (uygun olmayan geometrik biçimde ve yeterli kinetik enerjiye sahip olmayan
çarpışma) gerçekleşmiştir.
Ç)
a) Demirin paslanması
b) Kömürün yanması
c) Şimşek çakması
ç) Elmasın oluşumu
En hızlıdan en yavaşa doğru; şimşek çakması, kömürün yanması, demirin paslanması, elmasın oluşumu şeklinde sıralanır.
Öğrenci bu tepkimelerin hızlarını yorumlar.
D) Öğrenci iş sağlığı ve güvenliği açısından tehlikeli olan mesleklere örnekler yazacak. Tehlikeye sebep olan tepkimelere
örnek verecek.
Örnek: Maden İşçisi –Grizu patlaması
2.
1. Yönerge:
A)
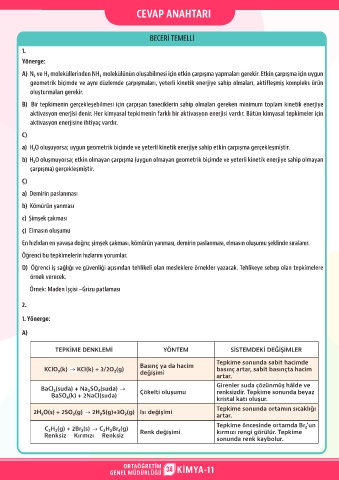
TEPKİME DENKLEMİ YÖNTEM SİSTEMDEKİ DEĞİŞİMLER
Tepkime sonunda sabit hacimde
Basınç ya da hacim
KClO₃(k) KCl(k) + 3/2O₂(g) basınç artar, sabit basınçta hacim
değişimi
artar.
Girenler suda çözünmüş hâlde ve
BaCl₂(suda) + Na₂SO₄(suda) Çökelti oluşumu renksizdir. Tepkime sonunda beyaz
BaSO₄(k) + 2NaCl(suda)
kristal katı oluşur.
Tepkime sonunda ortamın sıcaklığı
2H₂O(s) + 2SO₂(g) 2H₂S(g)+3O₂(g) Isı değişimi
artar.
Tepkime öncesinde ortamda Br₂'un
C₂H₂(g) + 2Br₂(s) C₂H₂Br₄(g) Renk değişimi kırmızı rengi görülür. Tepkime
Renksiz Kırmızı Renksiz
sonunda renk kaybolur.
ORTAÖĞRETİM 34 KİMYA-11
GENEL MÜDÜRLÜĞÜ