Page 90 - Kimya 10| Kavram Öğretimi Kitabı
P. 90
54 KİMYA 11
3. ÜNİTE SIVI ÇÖZELTİLER VE ÇÖZÜNÜRLÜK > 3.1. Çözücü Çözünen Etkileşimleri > 3.1.1. Kimyasal Türler Arası Etkileşimleri
Kullanarak Sıvı Ortamda Çözünme Olayı
Kavram : Çözünme Süreci
Genel Beceriler : Bilgi Okuryazarlığı Becerisi
Alan Becerileri : Çıkarım Yapma Becerisi
Çalışmanın Adı ÇÖZÜNME 15 dk.
Çalışmanın Amacı Çözünme olayını etkileşimler üzerinden açıklayabilme.
Yönerge: Aşağıda verilen bilgilerden yararlanarak soruları cevaplayınız.
Günlük hayatta bazı kelimeler cümle içinde yanlış anlamda kullanılmaktadır. Örneğin erime ve çözünme
kelimeleri. Erime olayı katı maddelerin ortamdan ısı alarak katı hâlden sıvı hâle geçmesidir. Buzdola-
bından çıkan buz oda sıcaklığındaki suda eriyerek hâl değiştirir. Erime olayı hâl değişimi olup fiziksel bir
o
değişmedir. Ayranın içine tuz atınca tuz erir mi? Yemek tuzunun erime sıcaklığı 801 C‘dir. Ayranımızın
sıcaklığı bu sıcaklıkta olmadığına göre tuz ayranda çözünerek gözle görülmeyecek şekilde dağılır.
Çözünme olayı çözünen maddenin çözücü içinde homojen dağılmasıyla oluşan bir olaydır. Peki bütün
maddeler birbiri içinde çözünebilir mi? Bu soruya günlük hayattan verilen örneklerle hayır cevabı veri-
lebilir. Zeytinyağı ve diğer yağ türleri suda çözünmezken, tuz, şeker, amonyak, etil alkol suda çözünür.
Çözünme olayı için; “Benzer benzeri çözer.” denebilir. Genel olarak polar çözücüler (en iyi bilinen su)
polar maddeleri, apolar çözücüler apolar maddeleri daha iyi çözer. Ayrıca iyonik yapılı bileşikler genel-
likle suda iyi çözünürler.
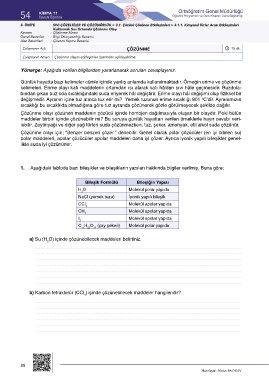
1. Aşağıdaki tabloda bazı bileşikler ve bileşiklerin yapıları hakkında bilgiler verilmiş. Buna göre;
Bileşik Formülü Bileşiğin Yapısı
H O Molekül polar yapıda
2
NaCl (yemek tuzu) İyonik yapılı bileşik
CCl Molekül apolar yapıda
4
CH Molekül apolar yapıda
4
I Molekül apolar yapıda
2
C H O (çay şekeri) Molekül polar yapıda
11 22 11
a) Su (H O) içinde çözünebilecek maddeleri belirtiniz.
2
b) Karbon tetraklorür (CCl ) içinde çözünebilecek maddeler hangileridir?
4
88
Hazırlayan: Harun BACANLI