Page 49 - Konu Özetleri AYT Kimya
P. 49
KIMYA
KONU KOLIGATIF ÖZELLIKLER
ÖZETİ
AYT AYT AYT AYT AYT AYT AYT AYT AYT AYT AYT AYT
ÇÖZELTILERIN KOLIGATIF ÖZELLIKLERI
Çözeltilerde çözünen maddenin (atom, iyon, molekül) sayısına ve derişimine bağlı olarak değişen özelliklere “koligatif
özellikler” denir.
BUHAR BASINCI ALÇALMASI
• Sabit sıcaklıkta kapalı bir kapta sıvısı ile dengede olan buharın basıncına “denge buhar basıncı” denir.
• Saf suya eklediğimiz madde sıvısının buharlaşmasına engel olacak şekilde sıvı yüzeyinde bulunacağından çözeltinin
buhar basıncı saf çözücünün buhar basıncından düşüktür. Çözünen maddenin derişimi arttıkça buhar basıncı düşer.
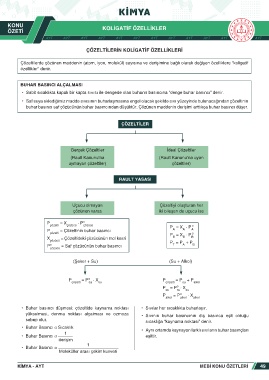
ÇÖZELTILER
Gerçek Çözeltiler İdeal Çözeltiler
(Rault Kanunu’na (Rault Kanunu’na uyan
uymayan çözeltiler) çözeltiler)
RAULT YASASI
Uçucu olmayan Çözeltiyi oluşturan her
çözünen varsa iki bileşen de uçucu ise
P = X · P o
çözelti çözücü çözücü P = X · P o
P = Çözeltinin buhar basıncı A A A
çözelti P = X · P o
X = Çözeltideki çözücünün mol kesri B B B
çözücü P = P + P
P o = Saf çözücünün buhar basıncı T A B
çözücü
(Şeker + Su) (Su + Alkol)
o
P = P · X P = P + P
çözelti su su çözelti su alkol
o
P = P · X
su su su
P = P o · X
alkol alkol alkol
• Buhar basıncı düşmesi; çözeltide kaynama noktası • Sıvılar her sıcaklıkta buharlaşır.
yükselmesi, donma noktası alçalması ve ozmoza • Sıvının buhar basıncının dış basınca eşit olduğu
sebep olur. sıcaklığa “kaynama noktası” denir.
• Buhar Basıncı α Sıcaklık • Aynı ortamda kaynayan farklı sıvıların buhar basınçları
1
• Buhar Basıncı α eşittir.
derişim
1
• Buhar Basıncı α
Moleküllerarası çekimkuvveti
KIMYA - AYT MEBİ KONU ÖZETLERİ 49