Page 53 - Konu Özetleri AYT Kimya
P. 53
ÇÖZÜNÜRLÜK VE ÇÖZÜNÜRLÜĞE ETKİ EDEN FAKTÖRLER
Çözünen Çözen Etkileşim Türü Açıklama
HCl H O Dipol - dipol Çözünür.
2
KCl H O İyon - dipol Çözünür.
2
Çok zayıf bir etkileşimdir, “çözünmez”
NaCl CCl İyon - indüklenmiş dipol
4 kabul edilir.
Zayıf bir etkileşimdir. Az da olsa çözünür.
O H O İndüklenmiş dipol - dipol
2 2 Sudaki hayatın kaynağıdır.
Çekim kuvvetleri birbirine yakındır.
I CCl İndüklenmiş dipol - indüklenmiş dipol (London)
2 4 Çözünür.
Hidrojen bağı, dipol dipolden daha etkindir.
NH H O Hidrojen bağı
3 2 Çözünür.
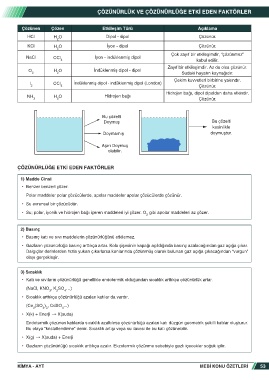
Bu çözelti
Doymuş Bu çözelti
kesinlikle
Doymamış doymuştur.
Aşırı Doymuş
olabilir.
ÇÖZÜNÜRLÜĞE ETKİ EDEN FAKTÖRLER
1) Madde Cinsi
• Benzer benzeri çözer.
Polar maddeler polar çözücülerde, apolar maddeler apolar çözücülerde çözünür.
• Su evrensel bir çözücüdür.
• Su; polar, iyonik ve hidrojen bağı içeren maddeleri iyi çözer. O gibi apolar maddeleri az çözer.
2
2) Basınç
• Basınç katı ve sıvı maddelerin çözünürlüğünü etkilemez.
• Gazların çözünürlüğü basınç arttıkça artar. Kola şişesinin kapağı açıldığında basınç azalacağından gaz açığa çıkar.
Dalgıçlar derinlerden hızla yukarı çıkarlarsa kanlarında çözünmüş olarak bulunan gaz açığa çıkacağından “vurgun”
olayı gerçekleşir.
3) Sıcaklık
• Katı ve sıvıların çözünürlüğü genellikle endotermik olduğundan sıcaklık arttıkça çözünürlük artar.
(NaCl, KNO , K SO …)
3 2 4
• Sıcaklık arttıkça çözünürlüğü azalan katılar da vardır.
(Ce (SO ) , CdSO ...)
2 4 3 4
• X(k) + Enerji † X(suda)
Endotermik çözünen katılarda sıcaklık azaltılırsa çözünürlüğü azalan katı düzgün geometrik şekilli katılar oluşturur.
Bu olaya “kristallendirme” denir. Sıcaklık artışı veya su ilavesi ile bu katı çözünebilir.
• X(g) † X(suda) + Enerji
• Gazların çözünürlüğü sıcaklık arttıkça azalır. Ekzotermik çözünme sebebiyle gazlı içecekler soğuk içilir.
KİMYA - AYT MEBİ KONU ÖZETLERİ 53