Page 42 - DEFTERİM KİMYA 10
P. 42
1. Ünite: Kimyanın Temel Kanunları ve Kimyasal Hesaplamalar
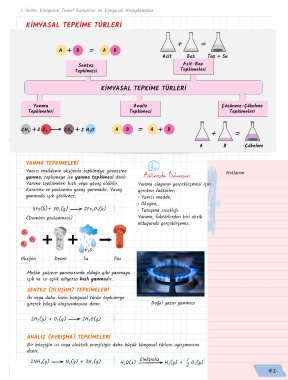
KİMYASAL TEPKİME TÜRLERİ
A B A B
Asit Baz Tuz + Su
Sentez Asit-Baz
Tepkimesi Tepkimeleri
KİMYASAL TEPKİME TÜRLERİ
Yanma Analiz Çözünme-Çökelme
Tepkimeleri Tepkimesi Tepkimeleri
2 H 2 O A B A B
CH 4 2 O 2 CO 2
A B Çökelme
YANMA TEPKİMELERİ
Yanıcı maddenin oksijenle tepkimeye girmesine Aklınızda Bulunsun Notlarım
yanma, tepkimeye ise yanma tepkimesi denir.
Yanma tepkimeleri hızlı veya yavaş olabilir. Yanma olayının gerçekleşmesi için
Kararma ve paslanma yavaş yanmadır. Yavaş gereken faktörler:
yanmada ışık görülmez. • Yanıcı madde,
• Oksijen,
4Fe(k)+ 3O 2 (g) 2Fe 2 O 3 (k) • Tutuşma sıcaklığı.
(Demirin paslanması) Yanma, faktörlerden biri eksik
olduğunda gerçekleşmez.
O 2
Fe
O 2
O 2
H 2 O
Oksijen Demir Su Pas
Metan gazının yanmasında olduğu gibi yanmaya
ışık ve ısı eşlik ediyorsa hızlı yanmadır.
SENTEZ (OLUŞUM) TEPKİMELERİ
İki veya daha fazla kimyasal türün tepkimeye
girerek bileşik oluşturmasına denir. Doğal gazın yanması
2H 2 (g) + O 2 (g) 2H 2 O(g)
ANALİZ (AYRIŞMA) TEPKİMELERİ
Bir bileşiğin ısı veya elektrik enerjisiyle daha küçük kimyasal türlere ayrışmasına
denir.
Elektroliz 1
2NH 3 (g) N 2 (g) + 3H 2 (g) H 2 O(s) H 2 (g) + O 2 (g)
2
41
41