Page 177 - Dört Dörtlük Konu Pekiştirme Testi - AYT KİMYA
P. 177
KİMYA
ÇÖZÜMLÜ
SORULAR
Tepkime Hızı - Tepkime Hızını Etkileyen Faktörler
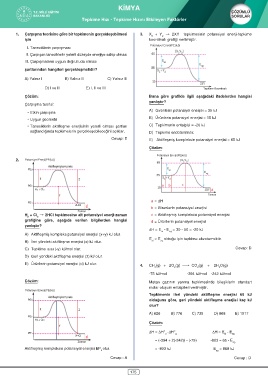
1. Çarpışma teorisine göre bir tepkimenin gerçekleşebilmesi 3. X + Y † 2XY tepkimesinin potansiyel enerji-tepkime
2 2
için koordinatı grafiği verilmiştir.
I. Taneciklerin çarpışması Potansiyel Enerji (PE(kJ))
II. Çarpışan taneciklerin yeterli düzeyde enerjiye sahip olması [X Y ]
65 2 2
III. Çarpışmaların uygun doğrultuda olması
E
şartlarından hangileri gerçekleşmelidir? ai E
35 ag
X +Y 2
2
A) Yalnız I B) Yalnız II C) Yalnız III
D) I ve III E) I, II ve III 15 2XY
Tepkime Koordinatı
Potansiyel Enerji (PE(kJ))
Çözüm:
Buna göre grafikle ilgili aşağıdaki ifadelerden hangisi
Çarpışma teorisi: [X Y ]
yanlıştır? 2 2
65
Potansiyel Enerji (PE(kJ))
• Etkin çarpışma
A) Girenlerin potansiyel enerjisi = 35 kJ
E
ai
• Uygun geometri [X Y ] E ag
35
B) Ürünlerin potansiyel enerjisi = 15 kJ
2 2
65
• Taneciklerin aktifleşme enerjisinin yeterli olması şartları X +Y 2
2
E
sağlandığında tepkimelerin gerçekleşebileceğini açıklar. C) Tepkimenin entalpisi = -20 kJ
ai
E
15 ag
35
Cevap: E D) Tepkime endotermiktir. 2XY
X +Y
2 2 Tepkime Koordinatı
E) Aktifleşmiş kompleksin potansiyel enerjisi = 65 kJ
a b c
15
Çözüm: 2XY d
Tepkime Koordinatı
2. Potansiyel Enerji (PE(kJ)) Potansiyel Enerji (PE(kJ))
[X Y ]
Aktifleşmiş kompleks 65 2 2
PE
3
E
X Z ai E ag
35
PE 2 X +Y 2
2
H +Cl
2 2
Y 15 a b c
2XY d
PE Tepkime Koordinatı
1 2HCl d
Zaman a = ¢H
Potansiyel Enerji (PE(kJ))
H + Cl † 2HCl tepkimesine ait potansiyel enerji-zaman b = Girenlerin potansiyel enerjisi
2 2
grafiğine göre, aşağıda verilen bilgilerden hangisi yanlıştır? c = Aktifleşmiş kompleksin potansiyel enerjisi
Aktifleşmiş kompleks
Potansiyel Enerji (PE(kJ))
PE
A) Aktifleşmiş kompleks potansiyel enerjisi (x+y) kJ olur. d = Ürünlerin potansiyel enerjisi
3
B) İleri yöndeki aktfileşme enerjisi (x) kJ olur. ¢H = E - E = 30 - 50 = -20 kJ
X
Z
ai
ag
Aktifleşmiş kompleks
PE E < E olduğu için tepkime ekzotermiktir.
C) Tepkime ısısı (-y) kJ/mol olur. ai ag
PE
3
2
H +Cl 2
X
Z
2
D) Geri yöndeki aktifleşme enerjisi (z) kJ olur. Cevap: D
Y
PE
E) Ürünlerin potansiyel enerjisi (d) kJ olur.
2
PE
H +Cl
1 2 2 2HCl d
Y Zaman 4. CH (g) + 2O (g) √ CO (g) + 2H O(g)
2
2
2
4
PE 1 -75 kJ/mol -394 kJ/mol -242 kJ/mol
Çözüm: 2HCl d Zaman Metan gazının yanma tepkimesinde bileşiklerin standart
Potansiyel Enerji (PE(kJ)) molar oluşum entalpileri verilmiştir.
Tepkimenin ileri yöndeki aktifleşme enerjisi 65 kJ
Aktifleşmiş kompleks olduğuna göre, geri yöndeki aktifleşme enerjisi kaç kJ
PE 3 olur?
X Z A) 626 B) 776 C) 739 D) 868 E) 1017
PE
2
H +Cl 2 Çözüm:
2
Y
¢H = ¢H° -¢H° ¢H = E - E
PE ü g ai ag
1 2HCl d
Zaman = (-394 + 2(-242)) - (-75) -803 = 65 - E
ag
Aktifleşmiş kompleksin potansiyel enerjisi EP olur. = -803 kJ E = 868 kJ
3 ag
Cevap : A Cevap : D
175