Page 292 - DEFTERİM KİMYA 10
P. 292
ÜNİTE III: ASİTLER, BAZLAR VE TUZLAR
1. BÖLÜM: ASİTLER VE BAZLAR
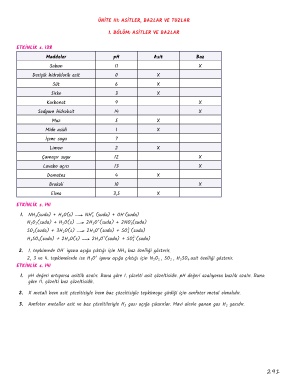
ETKİNLİK s. 138
Maddeler pH Asit Baz
Sabun 11 X
Derişik hidroklorik asit 0 X
Süt 6 X
Sirke 3 X
Karbonat 9 X
Sodyum hidroksit 14 X
Muz 5 X
Mide asidi 1 X
İçme suyu 7
Limon 2 X
Çamaşır suyu 12 X
Lavabo açıcı 13 X
Domates 4 X
Brokoli 10 X
Elma 3,5 X
ETKİNLİK s. 141
+
-
1. NH 3 (suda) + H 2 O(s) NH 4 (suda) + OH (suda)
+ -
N 2 O 5 (suda) + H 2 O(s) 2H 3 O (suda) + 2NO 3 (suda)
2-
+
SO 2 (suda) + 3H 2 O(s) 2H 3 O (suda) + SO 3 (suda)
2-
+
H 2 SO 4 (suda) + 2H 2 O(s) 2H 3 O (suda) + SO 4 (suda)
-
2. 1. tepkimede OH iyonu açığa çıktığı için NH 3 baz özelliği gösterir.
+
2, 3 ve 4. tepkimelerde ise H 3 O iyonu açığa çıktığı için N 2 O 5 , SO 2 , H 2 SO 4 asit özelliği gösterir.
ETKİNLİK s. 141
1. pH değeri artıyorsa asitlik azalır. Buna göre I. çözelti asit çözeltisidir. pH değeri azalıyorsa bazlık azalır. Buna
göre II. çözelti baz çözeltisidir.
2. X metali hem asit çözeltisiyle hem baz çözeltisiyle tepkimeye girdiği için amfoter metal olmalıdır.
3. Amfoter metaller asit ve baz çözeltileriyle H 2 gazı açığa çıkarırlar. Mavi alevle yanan gaz H 2 gazıdır.
291