Page 46 - Fen Lisesi Kimya 10 | 2. Ünite
P. 46
5. BÖLÜM GERÇEK GAZLAR
■ Günlük yaşamda hangi gazlar kullanılır?
■ Gazların hacimleri hangi durumlarda ihmal edilir?
■ Gerçek gazların ölçülen hacim ve basınçları ideal gaz denkleminde he-
saplanan hacim ve basınca eşit midir?
■ Buhar ile gaz kavramları arasındaki fark nedir?
■ Gerçek gazları ideal gazdan ayıran özellikler nelerdir?
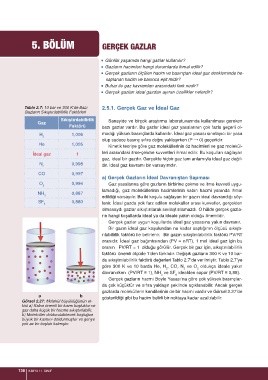
Tablo 2.7: 10 bar ve 300 K’de Bazı 2.5.1. Gerçek Gaz ve İdeal Gaz
Gazların Sıkıştırılabilirlik Faktörleri
Sıkıştırılabilirlik Sanayide ve birçok araştırma laboratuvarında kullanılması gereken
Gaz
Faktörü bazı gazlar vardır. Bu gazlar ideal gaz yasalarının çok fazla geçerli ol-
H 1,006 madığı yüksek basınçlarda kullanılır. İdeal gaz yasası sınırlayıcı bir yasa
2
olup sadece basınç sıfıra doğru yaklaşırken (P → 0) geçerlidir.
He 1,005
Kinetik teoriye göre gaz moleküllerinin öz hacimleri ve gaz molekül-
leri arasındaki itme-çekme kuvvetleri ihmal edilir. Bu koşulları sağlayan
İdeal gaz 1
gaz, ideal bir gazdır. Gerçekte hiçbir gaz tam anlamıyla ideal gaz değil-
N 0,998
2 dir. İdeal gaz kavramı bir varsayımdır.
CO 0,997
a) Gerçek Gazların İdeal Davranıştan Sapması
O 0,994 Gaz yasalarına göre gazların birbirine çekme ve itme kuvveti uygu-
2
lamadığı, gaz moleküllerinin hacimlerinin kabın hacmi yanında ihmal
NH 0,887
3
edildiği varsayılır. Bu iki koşulu sağlayan bir gazın ideal davrandığı söy-
SF 0,880
6 lenir. İdeal gazda yok farz edilen moleküller arası kuvvetler, gerçekten
olmasaydı gazlar sıkıştırılarak sıvılaştırılamazdı. O hâlde gerçek gazla-
rın hangi koşullarda ideal ya da ideale yakın olduğu önemlidir.
Gerçek gazlar uygun koşullarda ideal gaz yasasına yakın davranır.
Bir gazın ideal gaz koşulundan ne kadar saptığının ölçüsü sıkıştı-
rılabilirlik faktörü ile belirlenir. Bir gazın sıkıştırılabilirlik faktörü PV/RT
oranıdır. İdeal gaz bağıntısından (PV = nRT), 1 mol ideal gaz için bu
oranın PV/RT = 1 olduğu görülür. Gerçek bir gaz için, sıkıştırılabilirlik
faktörü önemli ölçüde 1’den farklıdır. Değişik gazların 300 K ve 10 bar-
da sıkıştırılabilirlik faktörü değerleri Tablo 2.7’de verilmiştir. Tablo 2.7’ye
göre 300 K ve 10 barda He, H , CO, N ve O oldukça ideale yakın
2 2 2
davranırken (PV/RT ≅ 1), NH ve SF idealden sapar (PV/RT ≅ 0,88).
3 6
Gerçek gazların hacmi Boyle Yasası’na göre çok yüksek basınçlar-
da çok küçüktür ve sıfıra yaklaşır şeklinde açıklanabilir. Ancak gerçek
gazlarda moleküllerin kendilerinin de bir hacmi vardır ve Görsel 2.27’de
a b
gösterildiği gibi bu hacim belirli bir noktaya kadar azaltılabilir.
Görsel 2.27: Molekül büyüklüğünün et-
kisi a) Kabın önemli bir kısmı boşluktur ve
gaz daha küçük bir hacme sıkıştırılabilir.
b) Moleküller doldurulabilecek boşluğun
büyük bir kısmını doldurmuştur ve geriye
çok az bir boşluk kalmıştır.
138 KİMYA 11. SINIF