Page 47 - Fen Lisesi Kimya 11 | 3. Ünite
P. 47
SIVI ÇÖZELTİLER VE ÇÖZÜNÜRLÜK
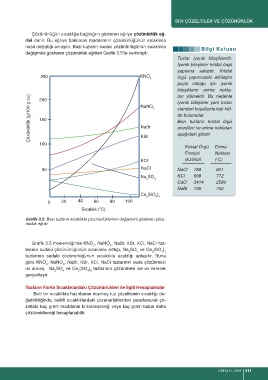
Çözünürlüğün sıcaklığa bağlılığını gösteren eğriye çözünürlük eğ-
risi denir. Bu eğriye bakılarak maddelerin çözünürlüğünün sıcaklıkla
nasıl değiştiği anlaşılır. Bazı tuzların sudaki çözünürlüğünün sıcaklıkla
Bilgi Kutusu
değişimini gösteren çözünürlük eğrileri Grafik 3.5’te verilmiştir.
Tuzlar iyonik bileşiklerdir.
İyonik bileşikler kristal örgü
yapısına sahiptir. Kristal
250 KNO 3 örgü yapısındaki etkileşim
güçlü olduğu için iyonik
bileşiklerin erime nokta-
ları yüksektir. Bu nedenle
Çözünürlük (g/100 g su) 150 NaNO 3 standart koşullarda katı hâl-
200
iyonik bileşikler yani tuzlar
de bulunurlar.
Bazı tuzların kristal örgü
NaBr
enerjileri ve erime noktaları
100 KBr aşağıdaki gibidir.
Kristal Örgü Erime
Enerjisi Noktası
o
KCI (kJ/mol) ( C)
50 NaCI NaCl 788 801
Na SO KCl 699 772
2 4
CaO 3414 2580
NaBr 736 750
Ce (SO )
2 4 3
0 20 40 60 80 100
o
Sıcaklık ( C)
Grafik 3.5: Bazı tuzların sıcaklıkla çözünürlüklerinin değişimini gösteren çözü-
nürlük eğrisi
Grafik 3.5 incelendiğinde KNO , NaNO , NaBr, KBr, KCl, NaCl tuz-
3 3
larının sudaki çözünürlüğünün sıcaklıkla arttığı, Na SO ve Ce (SO )
2 4 2 4 3
tuzlarının sudaki çözünürlüğünün sıcaklıkla azaldığı anlaşılır. Buna
göre KNO , NaNO , NaBr, KBr, KCl, NaCl tuzlarının suda çözünmesi
3 3
ısı alarak, Na SO ve Ce (SO ) tuzlarının çözünmesi ise ısı vererek
2 4 2 4 3
gerçekleşir.
Tuzların Farklı Sıcaklıklardaki Çözünürlükleri ile İlgili Hesaplamalar
Belli bir sıcaklıkta hazırlanan doymuş tuz çözeltisinin sıcaklığı de-
ğiştirildiğinde, belirli sıcaklıklardaki çözünürlüklerden yararlanarak çö-
zeltide kaç gram maddenin kristalleşeceği veya kaç gram tuzun daha
çözünebileceği hesaplanabilir.
211
KİMYA 11. SINIF