Page 15 - Kimya 12 | 2.Ünite
P. 15
3. BÖLÜM: DOĞADA KARBON
2.3.1. Karbon Elementinin Özellikleri
Atom numarası 6 olan ve periyodik tablonun 4A grubunda bulunan
karbon elementinin 4 tane değerlik elektronu vardır. Karbon elementi
değerlik elektronlarını aynı ya da farklı atomlarla ortaklaşa kullanarak
4 tane kovalent bağ yapar. Bu bağlar tekli olabileceği gibi ikili ya da
üçlü olabilir.
Karbonun oluşturabileceği bağ şekilleri aşağıda gösterilmiştir.
Karbon atomları arasında bağlar oluşurken açığa çıkan enerji fazla
olduğundan oluşan bu bağlar diğer atomların kendi aralarında yaptık-
ları bağlara göre daha kararlıdır.
Karbon elementi diğer atom veya atom gruplarıyla çok sayıda bağ
yapabilir. Karbon atomu düz ve dallanmış zincirli, halkalı, aromatik
yapıya sahip çok sayıda bileşik oluşturur.
Karbon elementinin oluşturiuğu bazı bileşikler V Viieo Bilgi
CH –CH –C=O CH –C–CH –CH 3 CH –CH –CH=CH–CH 3
3
2
3
2
3
2
OH O
O NH 2 CH 2 CH–CH
CH –C–O–CH –CH CH –CH–COOH CH 3 Karbonun Allotropları
3 2 3 3 2
CH
H C CH
H C CH CH –CH –C–H CH –CH –C C–CH–CH 3
2
3
3
2
CH O CH 3
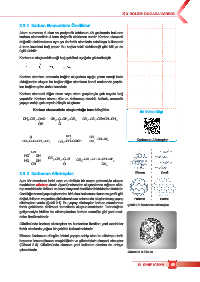
2.3.2. Karbonun Allotropları Elmas Grafit
Aynı tür atomların farklı sayı ve dizilişte bir araya gelmesiyle oluşan
maddelere allotrop denir. Aynı tür atomdan oluşmalarına rağmen allot-
rop maddelerin fiziksel ve bazı kimyasal özellikleri birbirinden farklıdır.
Canlılığın temel yapı taşlarından biri olan karbonun elmas ve grafit gibi
doğal, fulleren ve grafen gibi laboratuvar ortamında oluşturulmuş yapay Fulleren Grafen
allotropları vardır (Şekil 2.1). Bu yapay allotroplar karbon atomlarının Şekil 2.1: Karbonun allotropları
farklı şekillerde dizilmesi temelinde oluşturulmaktadır. Teknolojinin
gelişmesiyle birlikte bu allotroplardan karbon nanotüp gibi yeni mad-
deler üretilmektedir.
Günümüzde karbon allotropları ve bunlardan üretilen yeni maddeler
farklı alanlarda yoğun bir şekilde kullanılmaktadır.
Elmas: Karbonun düzgün kristal yapıya sahip olan bu allotropu tarih
boyunca insanoğlunun zenginliğinin ve gösterişinin simgesi olmuştur
(Görsel 2.3). Günümüzde elmasın yeni kullanım alanları da ortaya
çıkmaktadır.
Görsel 2.3: Elmas
12. SINIF KIMYA 97