Page 92 - Konu Özetleri AYT Kimya
P. 92
ELEKTROT POTANSIYELLERI
DERIŞIMI FARKLI HÜCRELER
V
�
2+
Cd (suda) + 2e † Cd(k) (�0,4 V)
Cd Sn Sn (suda) + 2e † Sn(k) (�0,14 V)
�
2+
İndirgenme potansiyeli küçük olan Cd daha aktiftir ve anottur.
0,01 M CdCI (suda) 0,1 M SnCI (suda)
2 2
0 0592, Anot
2+
0
(Yük = Anot) Cd(k) † Cd (suda) + 2e � E 0 = 0,4 V E E log
yük. pil pil n Katot
�
2+
(İnd = Katot) Sn (suda) + 2e † Sn(k) E 0 = �0,14 V
ind.
0 0592, 001,
,
0
2+
2+
Pil: Cd(k) + Sn (suda) † Cd (suda) + Sn(k) E = 0,26 V 026 log
pil. 2 01,
0
E = Standart pil gerilimi (Derişimler birer M olsaydı) = 0,26 + 0,0296
pil
= 0,2896 V
V
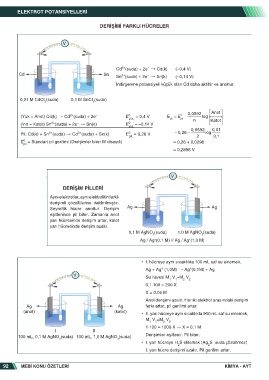
DERIŞIM PILLERI
Aynı elektrotlar, aynı elektrolitin farklı
derişimli çözeltilerine daldırılmıştır.
Seyreltik hücre anottur. Derişim Ag Ag
eşitlenince pil biter. Zamanla anot
yarı hücresinde derişim artar, katot
yarı hücresinde derişim azalır.
0,1 M AgNO (suda) 1,0 M AgNO (suda)
3 3
+
Ag / Ag (0,1 M) // Ag / Ag (1,0 M)
+
• I. hücreye aynı sıcaklıkta 100 mL saf su eklemek,
+
+
Ag + Ag (1,0M) † Ag (0,1M) + Ag
V Su ilavesi M V =M V
1 1 2 2
0,1·100 = 200·X
X = 0,05 M
Anot derişimi azalır. Her iki elektrot arasındaki derişim
Ag Ag farkı artar, pil gerilimi artar.
(anot) (katot)
• II. yarı hücreye aynı sıcaklıkta 900 mL saf su eklemek,
M V =M V
1 1 2 2
1·100 = 1000·X ¡ X = 0,1 M
I II
100 mL, 0,1 M AgNO (suda) 100 mL, 1,0 M AgNO (suda) Derişimler eşitlenir. Pil biter.
3 3
• I. yarı hücreye H S eklemek (Ag S suda çözünmez)
2 2
I. yarı hücre derişimi azalır. Pil gerilimi artar.
92 MEBİ KONU ÖZETLERİ KIMYA - AYT