Page 111 - Dört Dörtlük Konu Pekiştirme Testi - TYT KİMYA
P. 111
Kimyasal Türler ve Kimyasal Türler Arasındaki Etkileşimlerin
ÇÖZÜMLÜ SORULAR Sınıflandırılması KİMYA
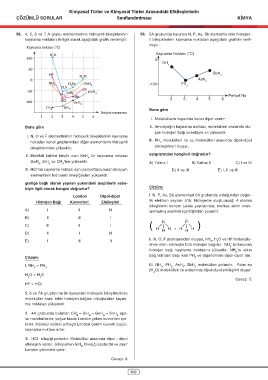
58. 4, 5, 6 ve 7 A grubu elementlerinin hidrojenli bileşiklerinin 59. 5A grubunda bulunan N, P, As, Sb elementlerinin hidrojen-
kaynama noktaları ile ilgili olarak aşağıdaki grafik verilmiştir. li bileşiklerinin kaynama noktaları aşağıdaki grafikte veril-
miştir.
Kaynama Noktası (°C)
0
NH
3
SbH
3
AsH 3
-100 PH 3
Periyot No
2 3 4 5 6
Buna göre
I. Moleküllerin hepsinde kalıcı dipol vardır.
Buna göre II. Amonyağın kaynama noktası, molekülleri arasında olu-
şan hidrojen bağı sebebiyle en yüksektir.
I. N, O ve F elementlerinin hidrojenli bileşiklerinin kaynama
noktaları kendi gruplarındaki diğer elementlerin hidrojenli III. PH molekülleri ile su molekülleri arasında dipol-dipol
3
bileşiklerinden yüksektir. etkileşimleri oluşur.
yargılarından hangileri doğrudur?
II. Molekül kütlesi büyük olan SnH ün kaynama noktası
4
GeH , SiH ve CH ’ten yüksektir.
4 4 4 A) Yalnız I B) Yalnız II C) I ve III
III. HCl'nin kaynama noktası aynı periyotta bulunan silisyum D) II ve III E) I, II ve III
elementinin hidrojenli bileşiğinden yüksektir.
grafiğe bağlı olarak yapılan yukarıdaki tespitlerin sebe-
biyle ilgili olarak hangisi doğrudur? Çözüm:
London Dipol-dipol I. N, P, As, Sb elementleri 5A grubunda olduğundan değer-
Hidrojen Bağı Kuvvetleri Etkileşimi lik elektron sayıları 5’tir. Hidrojenle oluşturacağı 4 atomlu
bileşiklerin benzer Lewis yapılarında, merkez atom ortak-
A) I II III lanmamış elektron içerdiğinden polardır.
B) II III I .. ..
( N , P )
C) III II I
H H H H H H
D) II I III
II. N, O, F atomlarından oluşan, NH , H O ve HF molekülle-
E) I III II 3 2
rinde etkin etkileşim türü hidrojen bağıdır. NH ’ te bulunan
3
hidrojen bağı kaynama noktasını yükseltir. NH 'te etkin
3
bağ hidrojen bağı iken PH ve diğerlerinde dipol-dipol’ dür.
Çözüm: 3
I. NH > PH III. NH , PH , AsH , SbH molekülleri polardır. Polar su
3
3
3
3
3 3
(H O) molekülleri ile aralarında dipol-dipol etkileşimi oluşur.
2
H O > H S
2 2
Cevap: E
HF > HCl
5, 6 ve 7A gruplarının ilk üyelerinin hidrojenli bileşiklerinde
moleküller arası etkin hidrojen bağları olduğundan kayna-
ma noktaları yüksektir.
II. 4A grubunda bulunan CH – SiH – GeH – SnH apo-
4 4 4 4
lar moleküllerdir, yoğun fazda London çekim kuvvetleri içe-
rirler. Molekül kütlesi arttıkça London çekim kuvveti büyür,
kaynama noktası artar.
III. HCl bileşiği polardır. Moleküller arasında dipol - dipol
etkileşimi vardır. Silisyumun SiH bileşiği apolardır ve zayıf
4
London çekimleri içerir.
Cevap: A
108 109