Page 23 - Konu Özetleri AYT Kimya
P. 23
ELEMENTLERİ TANIYALIM
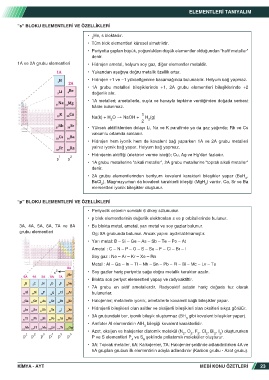
“s” BLOKU ELEMENTLERİ VE ÖZELLİKLERİ
• He, s bloktadır.
2
• Tüm blok elementleri küresel simetriktir.
• Periyotta çapları büyük, yoğunlukları düşük elementler olduğundan “hafif metaller”
denir.
1A ve 2A grubu elementleri • Hidrojen ametal, helyum soy gaz, diğer elementler metaldir.
• Yukarıdan aşağıya doğru metalik özellik artar.
• Hidrojen +1 ve �1 yükseltgenme basamağında bulunabilir. Helyum bağ yapmaz.
• 1A grubu metalleri bileşiklerinde +1, 2A grubu elementleri bileşiklerinde +2
değerlik alır.
• 1A metalleri; ametallerle, suyla ve havayla tepkime verdiğinden doğada serbest
hâlde bulunmaz.
1
Na(k) + H O † NaOH + H (g)
2 2
2
• Yüksek aktifliklerden dolayı Li, Na ve K parafinde ya da gaz yağında; Rb ve Cs
vakumlu ortamda saklanır.
• Hidrojen hem iyonik hem de kovalent bağ yaparken 1A ve 2A grubu metalleri
yalnız iyonik bağ yapar. Helyum bağ yapmaz.
• Hidrojenin aktifliği (elektron verme isteği); Cu, Ag ve Hg’dan fazladır.
• 1A grubu metallerine “alkali metaller”, 2A grubu metallerine “toprak alkali metaller”
denir.
• 2A grubu elementlerinden berilyum kovalent karakterli bileşikler yapar (BeH ,
2
BeCl ). Magnezyumun da kovalent karakterli bileşiği (MgH ) vardır. Ca, Sr ve Ba
2 2
elementleri iyonik bileşikler oluşturur.
“p” BLOKU ELEMENTLERİ VE ÖZELLİKLERİ
• Periyodik cetvelin sondaki 6 dikey sütunudur.
• p blok elementlerinin değerlik elektronları s ve p orbitallerinde bulunur.
3A, 4A, 5A, 6A, 7A ve 8A • Bu blokta metal, ametal, yarı metal ve soy gazlar bulunur.
grubu elementleri Og: 8A grubunda bulunur. Ancak yapısı aydınlatılmamıştır.
• Yarı metal: B – Si – Ge – As – Sb – Te – Po – At
Ametal : C – N – P – O – S – Se – F – Cl – Br – I
Soy gaz : Ne – Ar – Kr – Xe – Rn
Metal : Al – Ga – In – Tl – Nh – Sn – Pb – Fl – Bi – Mc – Lv – Ts
• Soy gazlar hariç periyotta sağa doğru metalik karakter azalır.
• Blokta son periyot elementleri yapay ve radyoaktiftir.
• 7A grubu en aktif ametallerdir. Radyoaktif astatin hariç doğada tuz olarak
bulunurlar.
• Halojenler; metallerle iyonik, ametallerle kovalent bağlı bileşikler yapar.
• Hidrojenli bileşikleri olan asitler ve oksijenli bileşikleri olan oksitleri sıkça görülür.
• 3A grubundaki bor, iyonik bileşik oluşturmaz (BH gibi kovalent bileşikler yapar).
3
• Amfoter Al elementinin AlH bileşiği kovalent karakterlidir.
3
• Azot, oksijen ve halojenler diatomik molekül (N , O , F , Cl , Bi , I ) oluştururken
2 2 2 2 2 2
P ve S elementleri P ve S şeklinde poliatomik moleküller oluşturur.
4 8
• 3A: Toprak metaller, 6A: Kalkojenler, 7A: Halojenler şeklinde adlandırılırken 4A ve
5A grupları grubun ilk elementinin adıyla adlandırılır (Karbon grubu - Azot grubu).
KİMYA - AYT MEBİ KONU ÖZETLERİ 23