Page 9 - Kimya 11 | Çalışma Defteri -7
P. 9
Hatırlıyor muyum?
Derişimin Tepkime Hızına Etkisi: Tepkime hızı etkin çarpışma sayısına bağlıdır.
Etkin çarpışma sayısını artıran faktörler tepkime hızını da artıracaktır. Etkin
çarpışma sayısını artıran faktörlerden biri de tepkimeye giren maddelerin
derişimidir. 1 M’lık HCl çözeltisi ile 2 M'lık HCl çözeltisinin 2,00 g Mg ile verdiği
tepkime karşılaştırıldığında 2 M'lık HCl çözeltisinin daha hızlı tepkime verdiği görülür. Hatırlıyorum
II. kaptaki tepkime I. kaptaki tepkimeden daha hızlı gerçekleşir çünkü derişim arttıkça 2 Puan
16 tepkime hızı da artar. Kısmen Hatırlıyorum
1 Puan
Hatırlamıyorum
0 Puan
1 M HCl 2 M HCl
2,00 g Mg 2,00 g Mg
Hatırlıyorum
2 Puan
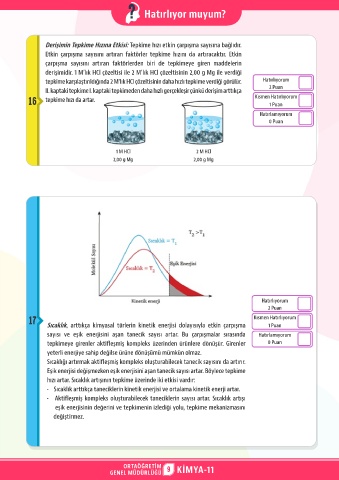
17 Sıcaklık, arttıkça kimyasal türlerin kinetik enerjisi dolayısıyla etkin çarpışma Kısmen Hatırlıyorum
1 Puan
sayısı ve eşik enerjisini aşan tanecik sayısı artar. Bu çarpışmalar sırasında Hatırlamıyorum
tepkimeye girenler aktifleşmiş kompleks üzerinden ürünlere dönüşür. Girenler 0 Puan
yeterli enerjiye sahip değilse ürüne dönüşümü mümkün olmaz.
Sıcaklığı artırmak aktifleşmiş kompleks oluşturabilecek tanecik sayısını da artırır.
Eşik enerjisi değişmezken eşik enerjisini aşan tanecik sayısı artar. Böylece tepkime
hızı artar. Sıcaklık artışının tepkime üzerinde iki etkisi vardır:
• Sıcaklık arttıkça taneciklerin kinetik enerjisi ve ortalama kinetik enerji artar.
• Aktifleşmiş kompleks oluşturabilecek taneciklerin sayısı artar. Sıcaklık artışı
eşik enerjisinin değerini ve tepkimenin izlediği yolu, tepkime mekanizmasını
değiştirmez.
MATEMATİK-11
ORTAÖĞRETİM 9 KİMYA-11
GENEL MÜDÜRLÜĞÜ