Page 4 - Kimya 11 | Çalışma Defteri -7
P. 4
Hatırlıyor muyum?
Tepkimeye girenlerin aktifleşmiş kompleks oluşturmaları için sahip olmaları
gereken en düşük enerjiye ileri tepkimenin aktifleşme enerjisi (Eai), ürünle-
rin aktifleşmiş kompleks oluşturmalarını sağlayacak en düşük enerjiye ise geri
tepkimenin aktifleşme enerjisi (Eag) denir. Reaksiyondaki net enerji değişimi
(ΔE veya ΔH) aktivasyon enerjileri farkı ile hesaplanır.
ΔE =ΔH = Eai - Eag
Aktifleşme enerjileri hiçbir zaman negatif değer alamaz. Ancak Eai'den Eag
çıkarıldığında elde edilen sonuç tepkime ekzotermikse negatif, endotermikse
pozitif değer alır. Endotermik ve ekzotermik tepkimelerin potansiyel enerji
tepkime koordinatı grafikleri de farklılık gösterir.
Hatırlıyorum
X₂(g) + Y₂(g) 2XY(g) + ısı
2 Puan
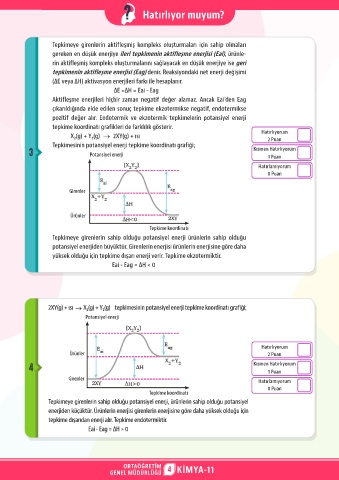
3 Tepkimesinin potansiyel enerji tepkime koordinatı grafiği; Kısmen Hatırlıyorum
Potansiyel enerji
1 Puan
Hatırlamıyorum
0 Puan
Girenler
Ürünler
Tepkime koordinatı
Tepkimeye girenlerin sahip olduğu potansiyel enerji ürünlerin sahip olduğu
potansiyel enerjiden büyüktür. Girenlerin enerjisi ürünlerin enerjisine göre daha
yüksek olduğu için tepkime dışarı enerji verir. Tepkime ekzotermiktir.
Eai - Eag = ΔH < 0
2XY(g) + ısı X₂(g) + Y₂(g) tepkimesinin potansiyel enerji tepkime koordinatı grafiği;
Potansiyel enerji
Hatırlıyorum
Ürünler 2 Puan
4 Kısmen Hatırlıyorum
1 Puan
Girenler
Hatırlamıyorum
0 Puan
Tepkime koordinatı
Tepkimeye girenlerin sahip olduğu potansiyel enerji, ürünlerin sahip olduğu potansiyel
enerjiden küçüktür. Ürünlerin enerjisi girenlerin enerjisine göre daha yüksek olduğu için
tepkime dışarıdan enerji alır. Tepkime endotermiktir.
Eai - Eag = ΔH > 0
ORTAÖĞRETİM 4 KİMYA-11
GENEL MÜDÜRLÜĞÜ