Page 90 - Kimya
P. 90
11. Sınıf Kimya
ÖRNEK VE ÇÖZÜM
1.
Potansiyel enerji Potansiyel enerji
aktifleşmiş aktifleşmiş
kompleks kompleks
E E
P P
3 3
X Z
Z X
E E
P P
2 H +Cl 2 H +Cl
2 2 2 2
Y Y
E E
P 1 2HCI P 1 2HCI
I Zaman II Zaman
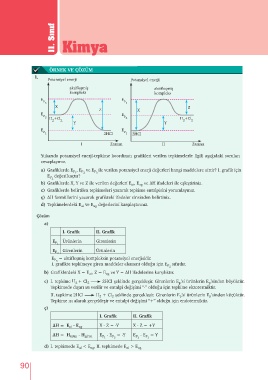
Yukarıda potansiyel enerji-tepkime koordinatı grafikleri verilen tepkimelerle ilgili aşağıdaki soruları
cevaplayınız.
a) Grafiklerde E , E ve E ile verilen potansiyel enerji değerleri hangi maddelere aittir? I. grafik için
P
3
P
P
2
1
E değeri kaçtır?
P
2
b) Grafiklerde X, Y ve Z ile verilen değerleri E , E ve ∆H ifadeleri ile eşleştiriniz.
ag
ai
c) Grafiklerde belirtilen tepkimeleri yazarak tepkime entalpisini yorumlayınız.
) ç ∆H formüllerini yazarak grafikteki ifadeler cinsinden belirtiniz.
d) Tepkimelerdeki E ve E değerlerini karşılaştırınız.
ai
ag
Çözüm
a)
I. Grafik II. Grafik
E P 1 Ürünlerin Girenlerin
Girenlerin
E
Ürünlerin
P
2
E = aktifleşmiş kompleksin potansiyel enerjisidir.
P
3
I. grafikte tepkimeye giren maddeler element olduğu için E sıfırdır.
P
2
b) Grafiklerdeki X = E , Z = E ve Y = ∆H ifadelerine karşılıktır.
ag
ai
c) I. tepkime H + Cl 2HCl şeklinde gerçekleşir. Girenlerin E ʼsi ürünlerin E ʼsinden büyüktür.
p
p
2
2
Tepkimede dışarı ısı verilir ve entalpi değişimi “-ˮ olduğu için tepkime ekzotermiktir.
II. tepkime 2HCl H + Cl şeklinde gerçekleşir. Girenlerin E ʼsi ürünlerin E ʼsinden küçüktür.
2
p
2
p
Tepkime ısı alarak gerçekleşir ve entalpi değişimi “+ˮ olduğu için endotermiktir.
) ç
I. Grafik II. Grafik
∆H = E - E ag X - Z = -Y X - Z = +Y
ai
∆H = H ürün - H giren E - E = -Y E - E = Y
P
P
P
P
2
1
1
2
d) I. tepkimede E < E , II. tepkimede E > E ag
ag
ai
ai
90