Page 95 - Kimya
P. 95
Kimya 11. Sınıf
ORTALAMA TEPKİME HIZI
Tepkimeye girenlerin madde miktarı tepkime başladığında en yüksek seviyededir. Tepkime ilerle-
dikçe girenler ürünlere dönüştüğü için ortamdaki tepkimeye giren madde miktarı azalır. Dolayısıyla etkin
çarpışma sayısı da azalır. Bu nedenle kimyasal tepkimelerde tepkime ilerledikçe tepkime hızı azalır.
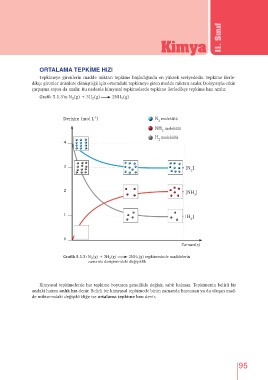
Grafik 5.1.3ʼte N (g) + 3H (g) 2NH (g)
3
2
2
-1
Derişim (mol L ) N molekülü
2
NH molekülü
3
H molekülü
2
4
3 [N ]
2
2
[NH ]
3
1
[H ]
2
0
Zaman(s)
Grafik 5.1.3: N 2 (g) + 3H 2 (g) 2NH 3 (g) tepkimesinde maddelerin
zamanla derişimindeki değişiklik
Kimyasal tepkimelerde hız tepkime boyunca genellikle değişir, sabit kalmaz. Tepkimenin belirli bir
andaki hızına anlık hız denir. Belirli bir kimyasal tepkimede birim zamanda harcanan ya da oluşan mad-
de miktarındaki değişiklikliğe ise ortalama tepkime hızı denir.
95