Page 4 - Fen Lisesi Kimya 11 | 6.Ünite
P. 4
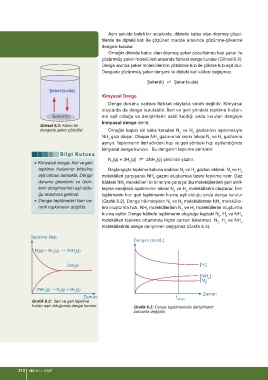
Aynı şekilde belirli bir sıcaklıkta, dibinde katısı olan doymuş çözel-
tilerde de dipteki katı ile çözünen madde arasında çözünme-çökelme
dengesi kurulur.
Örneğin dibinde katısı olan doymuş şeker çözeltisinde katı şeker ile
çözünmüş şeker molekülleri arasında fiziksel denge kurulur (Görsel 6.3).
Denge anında şeker moleküllerinin çözünme hızı ile çökme hızı eşit olur.
Dengede çözünmüş şeker derişimi ile dipteki katı kütlesi değişmez.
Şeker(k) ⇌ Şeker(suda)
Şeker(suda)
Kimyasal Denge
Denge durumu sadece fiziksel olaylarla sınırlı değildir. Kimyasal
olaylarda da denge kurulabilir. İleri ve geri yöndeki tepkime hızları-
Şeker(k) nın eşit olduğu ve derişimlerin sabit kaldığı anda kurulan dengeye
kimyasal denge denir.
Görsel 6.3: Katısı ile
dengede şeker çözeltisi Örneğin kapalı bir kaba konulan N ve H gazlarının tepkimesiyle
2 2
NH gazı oluşur. Oluşan NH gazının bir kısmı tekrar N ve H gazlarına
3 3 2 2
ayrışır. Tepkimenin ileri yöndeki hızı ile geri yöndeki hızı eşitlendiğinde
kimyasal denge kurulur. Bu dengenin tepkime denklemi
Bilgi Kutusu
N (g) + 3H (g) ⇌ 2NH (g) şeklinde yazılır.
■ Kimyasal denge, ileri ve geri 2 2 3
tepkime hızlarının birbirine Başlangıçta tepkime kabına sadece N ve H gazları eklenir. N ve H
2 2 2 2
eşit olması demektir. Denge molekülleri çarpışarak NH gazını oluşturmak üzere tepkime verir. Gaz
3
durumu girenlerin ve ürün- hâldeki NH molekülleri birbirleriyle çarpışır. Bu moleküllerden geri aktif-
3
lerin derişimlerinin eşit oldu- leşme enerjisini aşabilenler tekrar N ve H moleküllerini oluşturur. İleri
2 2
ğu anlamına gelmez. tepkimenin hızı geri tepkimenin hızına eşit olduğu anda denge kurulur
■ Denge tepkimeleri tam ve- (Grafik 6.2). Denge hâlindeyken N ve H moleküllerinin NH molekülle-
2 2 3
rimli tepkimeler değildir. rini oluşturma hızı, NH moleküllerinin N ve H moleküllerini oluşturma
3 2 2
hızına eşittir. Denge hâlinde tepkimenin oluştuğu kaptaki N , H ve NH
2 2 3
molekülleri tepkime ortamında hiçbir zaman tükenmez. N , H ve NH
2 2 3
moleküllerinin denge derişimleri değişmez (Grafik 6.3).
Tepkime Hızı
Derişim (mol/L)
N (g) + 3H (g) → 2NH (g)
2 2 3
Denge [H ]
2
[NH ]
3
[N ]
2
2NH (g) → N (g) + 3H (g)
3 2 2
Zaman
Zaman t denge
Grafik 6.2: İleri ve geri tepkime
hızları eşit olduğunda denge kurulur. Grafik 6.3: Denge tepkimesinde derişimlerin
zamanla değişimi
312 KİMYA 11. SINIF