Page 17 - Fen Lisesi Kimya 11 | 4. Ünite
P. 17
KİMYASAL TEPKİMELERDE ENERJİ
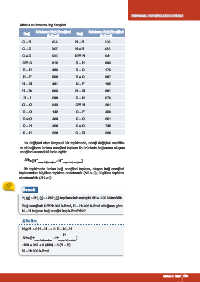
Tablo 4.6: Ortalama Bağ Enerjileri
Ortalama Bağ Enerjileri Ortalama Bağ Enerjileri
Bağ Bağ
(kJ/mol) (kJ/mol)
C − H 414 N − N 193
C − C 347 N = N 418
C = C 620 N ≡ N 941
C ≡ C 812 N − H 393
H − H 436 N − O 176
H − F 568 N = O 607
H − Cl 431 N − F 195
H − Br 366 N − Cl 381
H − I 298 C − N 276
Cl − Cl 243 C ≡ N 891
O − O 142 C − F 450
O = O 499 C − O 351
O − H 460 C = O 745
S − H 368 C − Cl 338
Isı değişimi olan kimyasal bir tepkimede, enerji değişimi reaktifle-
re ait bağların kırılma enerjileri toplamı ile ürünlerin bağlarının oluşma
enerjileri arasındaki farka eşittir.
o
∆H = [H o - H o ]
kırılan bağ enerjileri oluşan bağ enerjileri
Bir tepkimede kırılan bağ enerjileri toplamı, oluşan bağ enerjileri
toplamından büyükse tepkime endotermik (∆H > 0), küçükse tepkime
ekzotermiktir (∆H < 0).
Örnek
N (g) + 3H (g) → 2NH (g) tepkimesinin entalpisi ∆H = -109 kJ/mol’dür.
2 2 3
Bağ enerjileri: N ≡ N: 941 kJ/mol, H − H: 436 kJ/mol olduğuna göre
N − H bağının bağ enerjisi kaç kJ/mol’dür?
Çözüm
N ≡ N + 3 H − H → 2 H − N − H
H
o
o
o
∆H = [H - H ]
kırılan bağ enerjileri oluşan bağ enerjileri
-109 = 941 + 3.(436) – 6.(N − H)
N − H: 393 kJ/mol
251
KİMYA 11. SINIF