Page 26 - Kimya 12 | 1.Ünite
P. 26
1. ÜNITE: KIMYA VE ELEKTRIK
SHE kullanılarak standart indirgenme potansiyelleri belirlenen bazı
elementler aşağıda gösterilmiştir (Tablo 1.3):
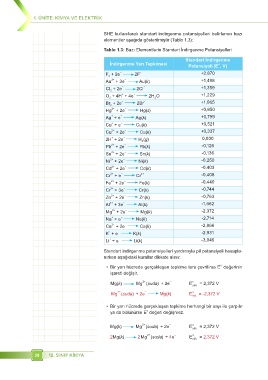
Tablo 1.3: Bazı Elementlerin Standart Indirgenme Potansiyelleri
Standart İndirgenme
İndirgenme Yarı Tepkimesi Potansiyeli (E , )
o
−
F + 2e 2F − +2,870
2
−
3+
Au + 3e Au(k) +1,498
−
CI + 2e 2CI − +1,359
2
+
O + 4H + 4e − 2H O +1,229
2
2
Br + 2e − 2Br − +1,065
2
2+
Hg + 2e − Hg(s) +0,850
+
Ag + e − Ag(k) +0,799
+
Cu + e − Cu(k) +0,521
2+
Cu + 2e − Cu(k) +0,337
+
2H + 2e − H (g) 0,000
2
2+
Pb + 2e − Pb(k) -0,126
2+
Sn + 2e − Sn(k) -0,136
2+
Ni + 2e − Ni(k) -0,250
2+
Cd + 2e − Cd(k) -0,403
3+
Cr + e − Cr 2+ -0,408
2+
Fe + 2e − Fe(k) -0,440
3+
Cr + 3e − Cr(k) -0,744
2+
Zn + 2e − Zn(k) -0,763
3+
Al + 3e − Al(k) -1,662
2+
Mg + 2e − Mg(k) -2,372
+
Na + e − Na(k) -2,714
2+
Ca + 2e − Ca(k) -2,866
+
K + e − K(k) -2,931
+
Li + e − Li(k) -3,040
Standart indirgenme potansiyelleri yardımıyla pil potansiyeli hesapla-
nırken aşağıdaki kurallar dikkate alınır.
o
• Bir yarı hücrede gerçekleşen tepkime ters çevrilirse E değerinin
işareti değişir.
–
Mg(k) Mg 2+ (suda + 2e E o ykü . = 2,372 V
)
−
o
Mg 2+ (suda + 2e Mg(k) E ind . = -2,372 V
)
• Bir yarı hücrede gerçekleşen tepkime herhangi bir sayı ile çarpılır
o
ya da bölünürse E değeri değişmez.
Mg(k) Mg 2+ (suda + 2e − E o ykü . = 2,372 V
)
2Mg(k) 2Mg 2+ (suda + 4e − E o ykü . = 2,372 V
)
38 12. SINIF KIMYA