Page 28 - Fen Lisesi Kimya 11 | 3. Ünite
P. 28
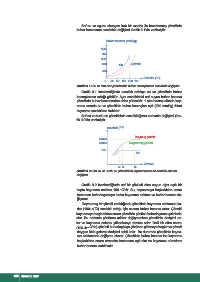
Saf su ve uçucu olmayan katı bir madde ile hazırlanmış çözeltinin
buhar basıncının sıcaklıkla değişimi Grafik 3.1’de verilmiştir.
Buhar basıncı (mmHg)
800
760
600
400 Su Çözelti
200
o
Sıcaklık ( C)
0 40 60 80 100 115
Grafik 3.1: Su ve katı-sıvı çözeltisinin buhar basınçlarının sıcaklıkla değişimi
Grafik 3.1 incelendiğinde sıcaklık arttıkça su ve çözeltinin buhar
basınçlarının arttığı görülür. Aynı sıcaklıktaki saf suyun buhar basıncı
çözeltinin buhar basıncından daha yüksektir. 1 atm basınç altında kay-
nama anında su ve çözeltinin buhar basınçları eşit (760 mmHg) fakat
kaynama sıcaklıkları farklıdır.
Saf su ve tuzlu su çözeltisinin sıcaklıklığının zamanla değişimi Gra-
fik 3.2’de verilmiştir.
o
Sıcaklık ( C)
Doymuş çözelti
100+b
100+a Doymamış çözelti
100
Su
Zaman
5t 6t 8t
Grafik 3.2: Saf su ve tuzlu su çözeltisinin kaynamasına ait sıcaklık-zaman
değişimi
Grafik 3.2 incelendiğinde saf bir çözücü olan suyun ağzı açık bir
o
kapta kaynama noktası 100 C’dir. Su, kaynamaya başladıktan sonra
tamamen buharlaşıncaya kadar kaynama noktası ve buhar basıncı de-
ğişmez.
Doymamış bir çözelti ısıtıldığında çözeltinin kaynama noktasına ka-
o
dar (100+a C) sıcaklık arttığı için sıvının buhar basıncı artar. Çözelti
kaynamaya başladıktan sonra çözeltide çözücü buharlaşması çok fazla
olur. Bu nedenle çözünen miktar değişmezken çözeltinin derişimi ar-
tar ve kaynama noktası yükselmeye devam eder. Belli bir süre sonra
(100+b C’de) çözücü buharlaştıkça çözünen çökmeye başlar ve çözelti
o
doygun hâle gelerek derişimi sabit kalır. Bu durumda çözeltinin kayna-
ma noktasında değişme olmaz. Çözeltinin buhar basıncı ise kaynama
başladıktan sonra atmosfer basıncına eşit olur ve kaynama süresince
buhar basıncı sabit kalır.
192 KİMYA 11. SINIF