Page 25 - Fen Lisesi Kimya 12 | 2.Ünite
P. 25
2.5.1. Çoklu Kovalent Bağ
Kovalent bağ oluşumunu açıklayan pek çok kuram vardır. Dikkat!
Bunlardan biri değerlik bağ kuramıdır. Bu kurama göre bir
atomdaki yarı dolu orbital ile diğer atomun yarı dolu orbitali
örtüştüğünde kimyasal bağ oluşur. Örtüşen bu iki orbitalde-
ki elektron sayısı ikiden fazla olamaz ve bu elektronlar her iki
atomda ortak hareket etmeye başlar. Molekülde sigma bağı
Bu kurama göre atomik orbitallerin örtüşmesi sonucu iki tür oluşmadan pi bağı oluşmaz.
kovalent bağ meydana gelebilir. Orbitaller molekül oluşturmak
üzere uç uca girişim yaparsa oluşan bağ sigma (σ) bağıdır. Sig-
ma bağında elektron yoğunluğu, iki atom arasında ve iki atomu
birleştiren doğru (bağ ekseni) üzerindedir. Sigma bağı iki atom
arasında meydana gelen ilk bağdır. İki atomlu moleküllerde
sigma bağları iki s orbitalinin, bir s orbitali ile bir p orbitalinin
veya iki p orbitalinin örtüşmesiyle meydana gelir. İki atomun p
orbitallerinin yan yana gelerek girişimde bulunması durumunda
pi (π) bağı oluşur. Böylelikle atomlar arasında ikili ve üçlü bağ-
lar meydana gelir. Sigma bağları pi bağlarına göre daha kararlı-
dır. Bu nedenle sigma bağlarını kırmak için gerekli olan enerji,
pi bağlarını kırmak için gerekli enerjiden daha fazladır.
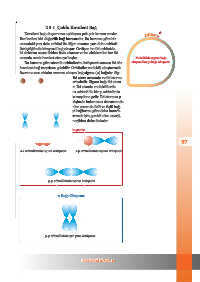
σ Bağı Oluşumu
97
s-s orbitallerinin uç uca örtüşmesi s-p orbitallerinin uç uca örtüşmesi
p-p orbitallerinin uç uca örtüşmesi
π Bağı Oluşumu
p-p orbitallerinin yan yana örtüşmesi
FEN LİSESİ KİMYA 12