Page 11 - Kimya 11 | 1.Ünite
P. 11
Z
Modern Atom Teorisi
p Orbitalleri
p orbitali çekirdeğin iki tarafında zıt yönel- Elektronların
bulunma olası-
miş iki ayrı lobdan oluşan elektron bulutudur. Aynı
lıklarının yüksek
enerji değerine karşılık gelen 3 tane p orbitali bu-
olduğu bölgeler
lunur (Görsel 1.1.10). Fakat bu p orbitallerinin
uzaydaki yönelişleri farklıdır. Elektron bu-
lutlarındaki lobutlar birbirine dik x, y,
z eksenleri üzerindeki p , p , p or-
y
x
z
bitalleri olarak belirtilir. Her bir or-
bital en fazla 2 elektron alabilece-
ği için p orbitali en fazla 6 elektron
alabilir. 2. enerji düzeyinden itiba-
ren üst enerji düzeylerinde bulunur. X
Y
Elektronların bulunma olasılık-
larının yüksek olduğu bölgelerin
oluşturduğu orbitallerin (p , p ,
y
x
p ) olası şekilleri
z
Z Z Z
X X X
Y Y Y
p p p
x y z
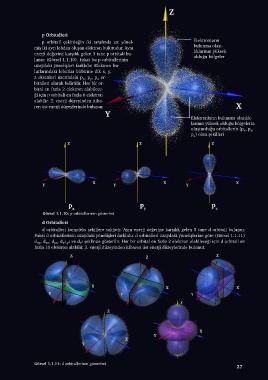
Görsel 1.1.10: p orbitallerinin gösterimi
d Orbitalleri
d orbitalleri kompleks şekillere sahiptir. Aynı enerji değerine karşılık gelen 5 tane d orbitali bulunur.
Fakat d orbitallerinin uzaydaki yönelişleri farklıdır. d orbitalleri uzaydaki yönelişlerine göre (Görsel 1.1.11)
d , d , d , d 2 2 ve d 2 şeklinde gösterilir. Her bir orbital en fazla 2 elektron alabileceği için d orbitali en
xz
xy
yz
z
x -y
fazla 10 elektron alabilir. 3. enerji düzeyinden itibaren üst enerji düzeylerinde bulunur.
Z Z Z
X X X
Y Y Y
Z
Z
X
Y
X
Y
Görsel 1.1.11: d orbitallerinin gösterimi
27
27