Page 29 - Kimya 11 | 1.Ünite
P. 29
Modern Atom Teorisi
İyonik yarıçap, iyonik bağlı bileşikteki bir iyonun yarıçapıdır. İyonik
bir bağdaki her atomun yarıçapı, kovalent bir bağdaki yarıçaptan fark- r katyon + r anyon
lıdır. Yarıçapın değişkenliğinin nedeni, iyonik bağdaki atomların farklı
boyutlara sahip olmalarıdır. İyonik bağlı bileşiklerde iyonlar aynı büyük- +
lükte değildir (Görsel 1.3.5). Bu nedenle iyon yarıçapı iyonlar arasında-
ki uzaklığın yarısı değildir. Çekirdekler arasındaki uzaklık katyon ve an-
yon arasında uygun şekilde paylaştırılarak ayrı ayrı hesaplanır. 1,40 �
2-
Görsel 1.3.6ʼda verilen CaO bileşiğinde Ca 2+ ve O çekirdekleri 2,40 �
2-
arasındaki uzaklık 2,40 Åʼdur. O nin yarıçapı 1,40 Å olduğuna göre
Ca 2+ un yarıçapı 2,40-1,40 =1,00 Å olur. Görsel 1.3.6: Kalsiyum oksit bileşiği-
nin iyonik yarıçapı
PERİYODİK ÖZELLİKLER
Atom veya İyon Yarıçapı
Periyodik sistemde aynı grupta yukarıdan aşağıya doğru atom yarı-
ÇÖZEREK ÖĞRENİN
çapı artar çünkü yukarıdan aşağıya doğru atomun elektron diziliminde
baş kuantum sayısı ve katman sayısı artar. Aynı periyotta soldan sağa
1. NaCl bileşiğinde iyon çekir-
doğru baş kuantum sayısı değişmez. Elektronlar aynı enerji seviyesi-
dekleri arasındaki uzaklık
ne yerleştiği hâlde proton sayısı (çekirdek yükü) arttığı için çekirdeğin -
2,83 Åʼdur. Cl ün iyon ya-
değerlik elektronlarına olan çekim gücü artar. Atom yarıçapı genellik-
rıçapı 1,81 Å olduğuna göre
le küçülür. +
Na un iyon yarıçapını bulu-
Geçiş elementlerinde ve iç geçiş elementlerinde atom yarıçapında-
nuz.
ki değişme miktarı beklenildiğinden azdır. Bunun nedeni elektronla-
rın son katmana değil, daha önceki alt katmana yerleşmesidir. Örneğin
4. periyotta geçiş metallerinin elektron dizilimi yapılırken elektronlar
önce 4s orbitaline daha sonra 3d orbitaline yerleşir. Bu nedenle alt kat-
mana yerleşen (3d orbitali) elektronlar üst katmandaki (4s orbitalinde-
ki) elektronlara etki eden çekim gücünü azaltarak perdeleme etkisi ya-
par. Bu nedenle yarıçapta soldan sağa doğru beklenildiği gibi büyük bir
azalma görülmez. Lantanitlerde ise atom yarıçapında belirgin fakat ya-
vaş bir azalma görülür (Lantanit büzülmesi).
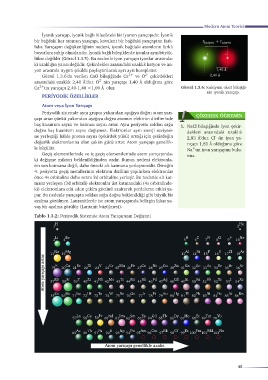
Tablo 1.3.2: Periyodik Sistemde Atom Yarıçapının Değişimi
H He
1 2
Li Be B C N O F Ne
3 4 5 6 7 8 9 10
Na 12 Mg 13 Al 14 Si 15 P 16 S 17 Cl 18 Ar
11
Atom yarıçapı artar. 37 Rb 20 Ca 21 Sc 40 Zr 41 Nb 42 Mo 25 Mn 44 Ru 27 Co 28 Ni 29 Cu 48 Cd 31 Ga 32 Ge 51 Sb 34 Se 35 Br 54 Xe
V
Fe
Cr
K
Kr
As
Ti
Zn
26
30
19
24
22
23
36
33
Te
Y
Sr
In
I
Sn
Rh
Tc
Ag
Pd
53
50
52
43
38
39
45
47
49
46
Cs Ba Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn
55 56 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86
La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb
57 58 59 60 61 62 63 64 65 66 67 68 69 70
Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No
89 90 91 92 93 94 95 96 97 98 99 100 101 102
Atom yarıçapı genellikle azalır.
45