Page 30 - Kimya 11 | 1.Ünite
P. 30
Modern Atom Teorisi
Tablo 1.3.2ʼden anlaşılacağı gibi periyodik sistemde aynı gruptaki
elementlerin atom yarıçapı yukarıdan aşağıya doğru artar. Aynı periyot-
ta soldan sağa doğru genellikle azalır, fakat soy gazların atom yarıçapı
bu azalma eğilimine uymaz.
Atom, elektron vererek katyon hâline geldiğinde en dıştaki elekt-
ronlar çekirdekten uzaklaşacağı için atomun katman sayısı azalabilir.
Kalan elektronlar çekirdek tarafından daha çok çekileceği için katyo-
nun yarıçapı nötr atomun yarıçapından küçük olur. Atom elektron ala-
rak anyon hâline geldiğinde ise elektron başına düşen çekim gücü aza-
lır. Dış tabaka genişler. Anyonun yarıçapı nötr atomun yarıçapından
büyük olur.
Katyonun iyon yarıçapı < Nötr atomun yarıçapı < Anyonun iyon yarıçapı
Örneğin azotun anyon, katyon ve nötr atomunun yarıçapları
karşılaştırıldığında
N N
7 7 7 N
2e - 2e - 5e - 2e - -
8e
N 5+ < N < N 3-
katyonun yarıçapının nötr atomdan küçük, anyonun yarıçapının nötr
atomdan büyük olduğu görülür.
ÇÖZEREK ÖĞRENİN
1. Aşağıda verilen kimyasal türlerin
yarıçaplarını karşılaştırınız. ( C)
6
4+ 2+ 4- 2-
C, C , C , C , C
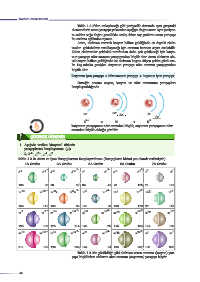
Tablo 1.3.3: Atom ve İyon Yarıçaplarının Karşılaştırılması (Yarıçapların birimi pm olarak verilmiştir.)
1A Grubu 2A Grubu 3A Grubu 6A Grubu 7A Grubu
+ 2+ 3+ -2 -
Li Li Be Be B B O F
3 3 4 4 5 5 8 O 8 5 F 5
134 90 90 59 82 41 73 126 71 119
Na Na + Mg Mg 2+ Al Al 3+ S 2- Cl -
11 11 12 12 13 13 16 S 16 17 Cl 17
154 116 130 86 118 68 102 170 99 167
+ 2+ 3+ -2 -
K K Ca Ca Ga Ga Se Br
19 19 20 20 31 31 34 Se 34 35 Br 35
196 152 174 114 126 76 116 184 114 182
+ 2+ 3+ 2- -
Rb Rb Sr Sr In In Te I
37 37 20 20 49 49 52 Te 52 53 I 53
211 166 192 132 144 94 135 207 133 206
Tablo 1.3.3ʼte görüldüğü gibi elektron veren atomun (katyon) yarı-
çapı küçülürken elektron alan atomun (anyonun) yarıçapı büyür.
46