Page 8 - Fizik 12 | 4.Ünite
P. 8
4. ÜNİTE: ATOM FİZİĞİNE GİRİŞ VE RADYOAKTİVİTE
Bulunan bu değerler kullanılarak atomun �ç enerj� sev�yeler� d�yagramı
elde ed�l�r (Şek�l 4.8).
E (eV)
İyonlaşma
0
-0,54 n = 5
-0,85 n = 4
-1,50 n = 3
-3,40 n = 2
-13,6 n = 1 (Temel hâl)
Şek�l 4.8: H�drojen atomunun enerj� sev�yeler�
Temel hâl (n = 1) düzey�ndek� elektronun n = 2, 3, 4 ... g�b� üst yörünge-
lere çıkması �ç�n atoma dışarıdan ver�lmes� gereken enerj�ye uyarılma
enerj�s� den�r.
Atomun �ç enerj� d�yagramından yola çıkılarak atomun uyarılması
�ç�n gerekl� enerj�ler ve bu enerj�ler� gösteren d�yagram elde ed�leb�l�r
(Şek�l 4.9).
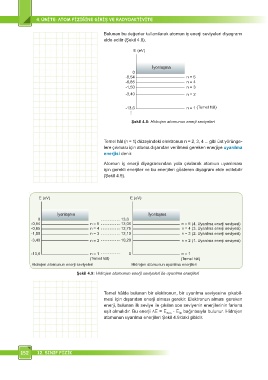
E (eV) E (eV)
İyonlaşma İyonlaşma
0 13,6
-0,54 n = 5 13,06 n = 5 (4. Uyarılma enerji seviyesi)
-0,85 n = 4 12,75 n = 4 (3. Uyarılma enerji seviyesi)
-1,50 n = 3 12,10 n = 3 (2. Uyarılma enerji seviyesi)
-3,40 n = 2 10,20 n = 2 (1. Uyarılma enerji seviyesi)
-13,6 n = 1 0 n = 1
(Temel hâl) (Temel hâl)
Hidrojen atomunun enerji seviyeleri Hidrojen atomunun uyarılma enerjileri
Şek�l 4.9: H�drojen atomunun enerj� sev�yeler� �le uyarılma enerj�ler�
Temel hâlde bulunan b�r elektronun, b�r uyarılma sev�yes�ne çıkab�l-
mes� �ç�n dışarıdan enerj� alması gerek�r. Elektronun alması gereken
enerj�, bulunan �lk sev�ye �le çıkılan son sev�yen�n enerj�ler�n�n farkına
eş�t olmalıdır. Bu enerj� ∆E = E Son - E bağıntısıyla bulunur. H�drojen
İlk
atomunun uyarılma enerj�ler� Şek�l 4.9’dak� g�b�d�r.
152 12. SINIF FİZİK