Page 289 - Öğretim Programı Okuryazarlığı
P. 289
Öğretim Programı Okuryazarlığı EK 4: Kimya 9 (9.3.3.1.-Anlama) Ders Planı Örneği
Tahminî Süre: 55 dakika
https://ogmmateryal.eba.gov.tr/panel/panel/EKitapUniteOnizle.aspx?Id=171&sayfa=108
Yukarıdaki linkte yer alan ders kitabından yararlanılarak atom ve iyonların Lewis sembollerinin çizimi açıklanır.
Bu bilgilerden yararlanarak keşfetme kısmında yer alan iyonik bağ oluşumu etkinliği (Etkinlik 1) öğretmen ile
birlikte tekrar yapılır. Öğrencilerin kendi cevaplarını buradakilerle karşılaştırarak amaçlanan öğrenme hede-
fine ulaşılması sağlanır.
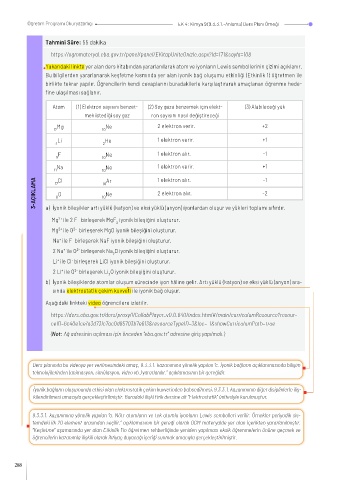
Atom (1) Elektron sayısını benzet- (2) Soy gaza benzemek için elekt- (3) Alabileceği yük
mek istediği soy gaz ron sayısını nasıl değiştireceği
Mg Ne 2 elektron verir. +2
12 10
Li He 1 elektron verir. +1
3 2
F Ne 1 elektron alır. -1
9 10
Na Ne 1 elektron verir. +1
11 Cl 10 Ar 1 elektron alır. -1
3-AÇIKLAMA 17 8 O 10 Ne 2 elektron alır. -2
18
a) İyonik bileşikler artı yüklü (katyon) ve eksi yüklü (anyon) iyonlardan oluşur ve yükleri toplamı sıfırdır.
2+
-
Mg ile 2 F birleşerek MgF iyonik bileşiğini oluşturur.
2
2+
Mg ile O birleşerek MgO iyonik bileşiğini oluşturur.
2-
+
Na ile F birleşerek NaF iyonik bileşiğini oluşturur.
-
2-
2 Na ile O birleşerek Na O iyonik bileşiğini oluşturur.
+
2
Li ile Cl birleşerek LiCl iyonik bileşiğini oluşturur.
+
-
2 Li ile O birleşerek Li O iyonik bileşiğini oluşturur.
+
2-
2
b) İyonik bileşiklerde atomlar oluşum sürecinde iyon hâline gelir. Artı yüklü (katyon) ve eksi yüklü (anyon) ara-
sında elektrostatik çekim kuvveti ile iyonik bağ oluşur.
Aşağıdaki linkteki video öğrencilere izletilir.
https://ders.eba.gov.tr/ders/proxy/VCollabPlayer_v0.0.840/index.html#/main/curriculumResource?resour-
ceID=6c40e1ce1a3d73fc7ac0d85703b7e613&resourceTypeID=3&loc=-1&showCurriculumPath=true
(Not: Ağ adresinin açılması için önceden “eba.gov.tr” adresine giriş yapılmalı.)
Ders planında bu videoya yer verilmesindeki amaç, 9.3.3.1. kazanımına yönelik yapılan “c. İyonik bağların açıklanmasında bilişim
teknolojilerinden (animasyon, simülasyon, video vb.) yararlanılır.” açıklamasının bir gereğidir.
İyonik bağların oluşumunda etkisi olan elektrostatik çekim kuvvetinden bahsedilmesi, 9.3.3.1. kazanımının diğer disiplinlerle iliş-
kilendirilmesi amacıyla gerçekleştirilmiştir. Buradaki ilişki fizik dersine ait “Elektrostatik” ünitesiyle kurulmuştur.
9.3.3.1. kazanımına yönelik yapılan “a. Nötr atomların ve tek atomlu iyonların Lewis sembolleri verilir. Örnekler periyodik sis-
temdeki ilk 20 element arasından seçilir.” açıklamasının bir gereği olarak OGM materyalde yer alan içerikten yararlanılmıştır.
“Keşfetme” aşamasında yer alan Etkinlik 1’in öğretmen rehberliğinde yeniden yapılması eksik öğrenmelerin önüne geçmek ve
öğrencilerin kazanımla ilişkili olarak ihtiyaç duyacağı içeriği sunmak amacıyla gerçekleştirilmiştir.
288
288