Page 151 - KİMYA-11
P. 151
Ortaöğretim Genel Müdürlüğü KİMYA 11
CEVAP ANAHTARLARI
2. Aynı periyotta p blokunda yer alan elementlerin yarıçapları s
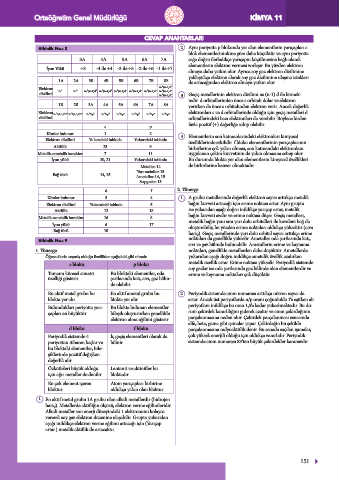
Etkinlik No.: 8
blok elementlerininkine göre daha küçüktür ve aynı periyotta
3A 4A 5A 6A 7A sağa doğru ilerledikçe yarıçapın küçülmesine bağlı olarak
elementlerin elektron vermesi zorlaşır. Bu yüzden elektron
İyon Yükü +3 -4 ile +4 -3 ile +5 -2 ile +6 -1 ile +7 almaya daha yatkın olur. Ayrıca soy gaz elektron dizilimine
yaklaştıkça elektron alarak soy gaz dizilimine ulaşma istekleri
1A 2A 3B 4B 5B 6B 7B 8B de artacağından elektron almaya yatkın olur.
ns2(n-1)d⁶
Elektron ns1 ns2 ns2(n-1)d1 ns2(n-1)d2 ns2(n-1)d3 ns1(n-1)d⁵ ns2(n-1)d⁵ ns2(n-1)d⁷
dizilimi ns2(n-1)d⁸ 3. Geçiş metallerinin elektron dizilimi ns (n-1) d ile bitmek-
tedir. d orbitallerinden önce s orbitali dolar ve elektron
1B 2B 3A 4A 5A 6A 7A 8A
verirken de önce s orbitalinden elektron verir. Ancak değerlik
Elektron ns1(n-1)d10 ns2(n-1)d10 ns2np1 ns2np2 ns2np3 ns2np⁴ ns2np⁵ ns2np⁶ elektronları s ve d orbitallerinde olduğu için geçiş metalleri d
dizilimi orbitallerindeki bazı elektronları da verebilir. Böylece birden
s p fazla pozitif (+) değerliğe sahip olabilir.
Kimler bulunur 1 2 4. Elementlerin son katmanlarındaki elektronları kimyasal
Elektron dizilimi Yukarıdaki tabloda Yukarıdaki tabloda özelliklerinde etkilidir. f bloku elementlerinin yarıçaplarının
Aktiflik 23 9 birbirlerine çok yakın olması, son katmandaki elektronlara
Metalik-ametalik karakter 7 11 uygulanan çekim kuvvetinin de yakın olmasına sebep olur.
İyon yükü 20, 21 Yukarıdaki tabloda Bu durumda blokta yer alan elementlerin kimyasal özellikleri
Metaller-14 de birbirlerine benzer olmaktadır.
Yarı metaller-15
Bağ türü 14, 15
Ametaller-14, 15
Soygazlar-13
d f 2. Yönerge
Kimler bulunur 3 4 1. A grubu metallerinde değerlik elektron sayısı arttıkça metalik
Elektron dizilimi Yukarıdaki tabloda 5 bağın kuvveti artacağı için erime noktası artar. Aynı grupta
Aktiflik 12 18 ise yukarıdan aşağı doğru inildikçe yarıçap artar, metalik
Metalik-ametalik karakter 16 8 bağın kuvveti azalır ve erime noktası düşer. Geçiş metalleri,
İyon yükü 6 17 metalik bağın yanı sıra yarı dolu orbitalleri ile kovalent bağ da
oluşturabilir, bu yüzden erime noktaları oldukça yüksektir (cıva
Bağ türü 10
hariç). Geçiş metallerinde yarı dolu orbital sayısı arttıkça erime
noktaları da genellikle yükselir. Ametaller oda şartlarında katı,
Etkinlik No.: 9
sıvı ve gaz hâlinde bulunabilir. Ametallerin erime ve kaynama
1. Yönerge noktaları, genellikle metallerden daha düşüktür. Ametallerde
Öğrencilerin seçmiş olduğu özellikler aşağıdaki gibi olmalı: yukarıdan aşağı doğru inildikçe ametalik özellik azalırken
s bloku p bloku metalik özellik artar. Erime noktası yükselir. Periyodik sistemde
soy gazlar ise oda şartlarında gaz hâlinde olan elementlerdir ve
Tamamı küresel simetri Bu bloktaki elementler, oda erime ve kaynama noktaları çok düşüktür.
özelliği gösterir. şartlarında katı, sıvı, gaz hâlin-
de olabilir.
En aktif metal grubu bu En aktif ametal grubu bu 2. Periyodik sistemde atom numarası arttıkça nötron sayısı da
blokta yer alır. blokta yer alır. artar. Ancak üst periyotlarda n/p oranı çoğunlukla 1’e eşitken alt
Bulundukları periyotta yarı- Bu blokta bulunan elementler periyotlara inildikçe bu oran 1,5’e kadar yükselmektedir. Bu du-
çapları en büyüktür. bileşik oluştururken genellikle rum çekirdek kararlılığını giderek azaltır ve atom çekirdeğinin
elektron alma eğilimi gösterir. parçalanmasına neden olur. Çekirdek parçalanması esnasında
alfa, beta, gama gibi ışımalar yapar. Çekirdeğin bu şekilde
d bloku f bloku parçalanmasına radyoaktiflik denir. Bu esnada saçılan ışımalar,
Periyodik sistemde 4. İç geçiş elementleri olarak da çok yüksek enerjili olduğu için oldukça zararlıdır. Periyodik
periyottan itibaren başlar ve bilinir. sistemde atom numarası 83’ten büyük çekirdekler kararsızdır.
bu bloktaki elementler, bile-
şiklerinde pozitif değişken
değerlik alır.
Özkütleleri büyük olduğu Lantanit ve aktinitler bu
için ağır metaller de denilir. bloktadır.
En çok element içeren Atom yarıçapları birbirine
bloktur. oldukça yakın olan bloktur.
1. En aktif metal grubu 1A grubu olan alkali metallerdir (hidrojen
hariç). Metallerde aktifliğin ölçüsü, elektron verme eğilimleridir.
Alkali metaller son enerji düzeyindeki 1 elektronunu kolayca
vererek soy gaz elektron düzenine ulaşabilir. Grupta yukarıdan
aşağı inildikçe elektron verme eğilimi artacağı için (Yarıçap
artar.) metalik aktiflik de artacaktır.
151