Page 9 - Fen Lisesi Kimya 9 | 4. Ünite
P. 9
MADDENİN HÂLLERİ
− +
Yani her Cl iyonu altı tane Na iyonu ile sarılmıştır. Bu nedenle, NaCl
formülü sodyum klorürün basit formülüdür.
Katyon ve anyonlar bileşikte elektriksel açıdan nötr olacak şekilde di-
zilir. İyonik bileşiklerin formülleri yazılırken katyon ve anyonların yükleri
gösterilmez (Şekil 4.5 a,b).
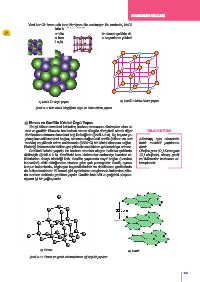
b) NaCl’ün birim hücre yapısı
a) NaCl’ün örgü yapısı
Şekil 4.5: Katı NaCl bileşiğinin örgü ve birim hücre yapısı
ç) Elmas ve Grafitin Kristal Örgü Yapısı
En iyi bilinen kovalent kristaller, karbon atomunun allotropları olan el-
mas ve grafittir. Elmasta her karbon atomu düzgün dört yüzlü olarak diğer BİLGİ KUTUSU
dört karbon atomuna kovalent bağ ile bağlıdır (Şekil 4.6 a). Üç boyuta ya-
yılmış kuvvetli kovalent bağlar, elmasın olağanüstü sertlik (bilinen en sert Allotrop; aynı elementin
madde) ve yüksek erime noktasında (3550 C) bir kristal olmasını sağlar. farklı molekül yapılarına
o
Elektriği iletmemekle birlikte çok yüksek sıcaklıklara çıkılmadıkça erimez. denir.
Grafitteki kristal yapıda ise karbon atomları altıgen halkalar şeklinde Oksijen gazı (O )-Ozon gazı
2
dizilmiştir (Şekil 4.6 b). Grafitteki bazı elektronlar serbestçe hareket et- (O ) oksijenin, elmas, grafit
3
tiklerinden dolayı elektriği iletir. Grafitin yapısında zayıf bağlar (London ve fullerenler karbonun al-
kuvvetleri) etkili olduğundan elmasa göre çok yumuşaktır. Grafit, ayrıca lotroplarıdır.
kurşun kalemlerde, bilgisayar kaydedicilerinin ve daktiloların şeritlerinde
de kullanılmaktadır. El feneri gibi aydınlatma araçlarında kullanılan pille-
rin merkez elektrotu grafitten yapılır. Grafitin katı hâli ve yağdaki süspan-
siyonu iyi bir yağlayıcıdır.
a) Elmas
b) Grafit
Şekil 4.6 : Elmas ve grafit allotroplarının ağ örgülü yapıları
149